В чем разница между электролитическими и гальваническими элементами? (Подробный анализ) - Все различия

Оглавление
Наука творила много чудес в прошлом, творит в настоящем и готовится к будущему. Слово "наука" произошло от латинского слова "Scientia", что означает знание; это знание основано на гипотезах, наблюдениях и экспериментах универсальной науки.
Как и в химии, здесь обсуждается движение ионов, для чего требуются различные типы ячеек. Устройство, преобразующее химическую энергию в электрическую или наоборот путем окислительно-восстановительной реакции, называется электрохимической ячейкой. Электрохимические ячейки бывают электролитические и гальванические (вольтовы элементы).
Электролитический элемент - это элемент, который состоит из положительного и отрицательного полюсов, известных как анод и катод. С другой стороны, гальванический элемент определяется как электрохимический элемент, который используется для преобразования химической энергии спонтанных окислительно-восстановительных реакций в электрическую энергию.
Электролитическая ячейка используется для процесса электролиза, который представляет собой процесс прохождения тока через электролит, благодаря чему происходит миграция отрицательных и положительных ионов к аноду и катоду.
Смотрите также: В чем разница между городом и поселком? (глубокое погружение) - Все различияГальванический элемент, также называемый вольтовым элементом, - это электрохимический элемент, в котором для получения электрической энергии используются химические реакции.
Обе эти камеры до сих пор так же полезны, как и во времена их изобретения, а это значит, что они не потеряли своей ценности в современном революционном обществе.
Важность и различия между гальваническими, или вольтаическими, и электролитическими элементами подробно обсуждаются в этой статье.
Электролитическая ячейка: как она работает?
Электролитическое устройство, использующее электрическую энергию для вызывания неспонтанной окислительно-восстановительной реакции, называется электролитической ячейкой. Определенные химические вещества могут быть подвергнуты электролизу с помощью электролитических ячеек, которые затем называются электрохимическими ячейками.

Электролитические элементы и конденсаторы
Например, вода может быть подвергнута электролизу для получения газообразного кислорода и газообразного водорода с помощью электролитического элемента. Это достигается за счет использования потока электронов (в реакционную среду) для преодоления барьера энергии активации неспонтанной окислительно-восстановительной реакции.
Основными частями электролитических ячеек являются:
- Катод (отрицательный заряд)
- Анод (положительный заряд)
- Электролит
Диссоциированные положительные ионы в электролите притягиваются к катоду электролитической ячейки при прохождении через нее внешнего электрического тока, в результате чего положительно заряженные ионы оседают на катоде.
К положительно заряженному аноду одновременно приближаются отрицательно заряженные ионы.
Что такое гальванический элемент и как он работает?
Гальванический или вольтаический элемент - это устройство, которое преобразует химическую энергию в электрическую энергию Гальванический элемент - это электрохимическое устройство, которое создает электричество посредством химических операций.
Смотрите также: В чем разница между потенцией атаки и силой удара (у вымышленных персонажей) - Все различияОбычный аппарат состоит из двух различных электродов.
Один состоит из меди, а другой - из цинка; оба помещены в отдельные мензурки, содержащие ионы соответствующих металлов в растворе, которые соединены солевым мостиком и разделены пористой мембраной.
Целью производства электролитических элементов является преобразование электрической энергии в химическую путем воздействия электролита на два металла, заряженных и соединенных в батарею, соответственно.
Причина производства гальванических элементов или вольтовых элементов заключается в том, что они способны преобразовывать химическую энергию в электрическую, которая необходима для рабочих целей.
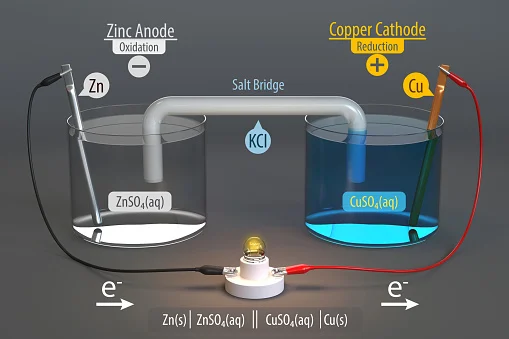
Эксперимент с гальваническим элементом
Различия между гальваническими и электролитическими элементами
Электролитические и гальванические элементы обладают некоторыми контрастными характеристиками, которые приведены в таблице ниже.
| Характеристики | Электролитическая ячейка | Гальванический или вольтаический элемент |
|---|---|---|
| Производство | В электролитической ячейке используется сосуд, заполненный электролитом, в который погружены два электрода, соединенные с батареей, соответственно анод и катод. | Гальванический элемент или вольтаический элемент получается, когда две мензурки наполнены электролитом и два электрода погружены в этот раствор. Эти мензурки соединены солевым мостиком, а оба электрода соответственно соединены батареей. |
| Энергия | Электролитическая ячейка преобразует электрическую энергию в химическую посредством окислительно-восстановительной реакции, которая происходит спонтанно и отвечает за производство электрической энергии. | Гальванический или вольтаический элемент - это элемент, преобразующий химическую энергию в электрическую посредством окислительно-восстановительной реакции, которая очень полезна для рабочих целей. |
| Источник энергии | Для работы электролитического элемента необходим внешний источник энергии. Батарея подключается к обоим электродам, что запускает работу электролитического элемента. | Гальванический или вольтаический элемент не требует внешнего источника энергии, так как сам производит энергию. |
| Обвинения | Электролитическая ячейка содержит отрицательно заряженные аноды и положительно заряженные катоды. | Гальванический элемент или вольтаический элемент содержит положительно заряженный анод и отрицательно заряженный катод. |
| Реакции | Электролитические элементы используют спонтанные реакции для получения химической энергии. Они преобразуют электрическую энергию в химическую. | Гальванические или вольтаические элементы используют неспонтанные реакции для получения электрической энергии. они преобразуют химическую энергию в электрическую, необходимую для работы. |
Различия между гальваническими и электролитическими элементами
Практическое применение электролитической ячейки
Электролитический элемент играет важную роль в современном обществе и используется массово. Практичность и важность электролитических элементов перечислены ниже:
- Он используется для получения металлического натрия из расплавленного хлорида натрия с помощью ячейки Даунса.
- Это используется для получения хлора га и приготовить каустическую соду (NaOH) из водного хлорида натрия с помощью ячейки Нельсона.
- Он используется для извлечения металлического алюминия.
- Он используется в электрорафинировании меди.
- Электролитические ячейки используются для гальванического покрытия металлов.
- Электролитическая ячейка используется для получения газообразного кислорода и газообразного водорода из воды путем ее электролиза.
Практическое применение гальванических или вольтаических элементов
Гальванические или вольтаические элементы являются важным изобретением для современного мира и используются человечеством повсеместно. Электричество - это основная необходимость современной жизни, а его производство - один из самых сложных процессов, однако у нас есть так много способов получения электроэнергии.
Гальванические или вольтаические элементы - один из самых ранних методов получения электроэнергии, который до сих пор имеет большое значение среди новых и современных методов получения электроэнергии.
- Процесс образования гальванических элементов имеет множество типов и оказывает большое влияние на жизнь человека. Сухие элементы или батарейки, которые мы часто используем в повседневной жизни, питают наши фонарики, телевизоры, игровые контроллеры и многие другие вещи.
- Свинцовая аккумуляторная батарея также является повседневным примером гальванического элемента. Функция свинцовой аккумуляторной батареи заключается в выработке электроэнергии при отключении основного источника питания. Она обычно используется в качестве резервной батареи в домах и на рабочих местах.
- Топливные элементы широко используются в промышленности, так как резервные мощности должны быть больше. Они используются, когда электричества нет, а оборудование должно работать.
Гальванический элемент против электролитического элемента
Заключение
- Подводя итог, можно сказать, что и электролитические, и гальванические, или вольтовы, элементы имеют свое значение в современном мире в своем собственном уникальном способе обработки. Оба эти элемента все еще используются и продолжают служить своей цели.
- В целом, метод, по которому производятся как электролитические, так и гальванические элементы, прост и легко доступен для обычного человека.
- Электролитический элемент не может работать, если он не подключен к внешнему источнику питания. В отличие от него, гальванический элемент не нужно подключать к внешнему источнику питания, так как он вырабатывает собственную энергию.
- Использование обеих камер теперь известно и привычно во всем мире, и это замечательное изобретение вошло в программу обучения молодежи и преподается каждому ребенку в наше время.

