Која је разлика између електролитичких ћелија и галванских ћелија? (Детаљна анализа) – Све разлике

Преглед садржаја
Наука је учинила многа чуда у прошлости, а свет ради у садашњости и спрема се за будућност. Реч „наука“ је преузета од латинске речи „Сциентиа“, што значи знање; ово знање је засновано на хипотезама, запажањима и експериментима универзалне науке.
Као и у хемији, расправља се о кретању јона за које су потребне различите врсте ћелија. Уређај који трансформише хемијску енергију у електричну енергију или обрнуто редокс реакцијом познат је као електрохемијска ћелија. Електрохемијске ћелије су електролитичке и галванске (волтаичне ћелије).
Електролитичка ћелија је ћелија која се састоји од позитивних и негативних полова познатих као анода и катода. С друге стране, галванска ћелија се дефинише као електрохемијска ћелија која се користи за претварање хемијске енергије спонтаних редокс реакција у електричну енергију.
Електролитичка ћелија се користи за процес електролизе, што је процес проласка струје кроз електролит. Због тога се одвија миграција негативних и позитивних јона ка аноди и катоди.
Галванска ћелија, такође названа волтаична ћелија, је електрохемијска ћелија која користи хемијске реакције за генерисање електричне енергије.
Обе ове ћелије су и даље корисне као што су биле у време њиховог проналаска, што значи да нису изгубиле своју вредносту данашњем револуционарном друштву.
О важности и разликама између галванских ћелија, или волтаичких ћелија, и електролитских ћелија се опширно говори у овом чланку.
Електролитичка ћелија: Како функционише?
Електролитички уређај који користи електричну енергију да изазове не-спонтану редокс реакцију познат је као електролитичка ћелија. Одређене хемикалије се могу електролизовати помоћу електролитичких ћелија, које се тада називају електрохемијске ћелије.

Електролитичке ћелије и кондензатори
На пример, вода се може електролизовати да би се створио гасовити кисеоник и гасовити водоник уз коришћење електролитичке ћелије. Ово се постиже коришћењем протока електрона (у реакционо окружење) како би се пробила енергетска баријера активације не-спонтане редокс реакције.
Главни делови електролитичких ћелија су:
- Катода (негативно наелектрисање)
- Анода (позитивно наелектрисање)
- Електролит
Дисоцирани позитивни јони у електролиту се привлаче на катоду електролитичка ћелија када кроз њу тече спољашња електрична струја. Ово узрокује да се позитивно наелектрисани јони таложе на катоди.
Позитивно наелектрисаној аноди се истовремено приближавају негативно наелектрисани јони.
Шта је галванска ћелија и како она функционише?
Галванска или волтаична ћелија је уређај који претварахемијску енергију у електричну енергију кроз насумичне редокс реакције. Галванска ћелија је електрохемијски уређај који ствара електричну енергију хемијским операцијама.
Заједнички апарат се састоји од две различите електроде.
Такође видети: Која је главна разлика између руског и белоруског језика? (Детаљно) – Све разликеЈедан је направљен од бакра, а други је цинк; обе су смештене у одвојене чаше које садрже одговарајуће металне јоне у раствору, који су повезани мостом соли и одвојени порозном мембраном.
Сврха производње електролитичких ћелија је претварање електричне енергије у хемијску излагањем електролита два метала напуњена и повезана са батеријом, респективно.
Узрок производње електролита. галванске ћелије или волтаичне ћелије је да су способне да претварају хемијску енергију у електричну енергију, која је потребна за рад.
Такође видети: Виндовс 10 Про вс. Про Н- (Све што треба да знате) – све разлике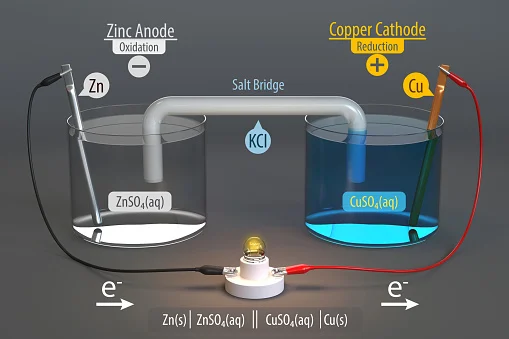
Експеримент са галванским ћелијама
Чињенице о разликовању између галванских и електролитичких ћелија
Електролитичке ћелије и галванске ћелије имају неке контрастне карактеристике о којима се говори у табели испод.
| Карактеристике | Електролитичка ћелија | Галванска или волтаична ћелија |
|---|---|---|
| Производња | Електролитичка ћелија користи посуду која је напуњена електролитима и у њега су умочене две електроде које су повезане са батеријом, односно чинећи их анодом икатода. | Галванска ћелија или волтаична ћелија настаје када се две чаше напуњене електролитима и две електроде уроне у овај раствор. Ове чаше су повезане мостом соли, а обе електроде су повезане батеријом. |
| Енергија | Електролитичка ћелија претвара електричну енергију у хемијску енергију кроз редокс реакцију која је спонтана и задужена је за производњу електричне енергије. | Галванска или волтаична ћелија је ћелија која трансформише хемијску енергију у електричну кроз редокс реакцију која је веома корисна за радне сврхе. |
| Извор енергије | Електролитичкој ћелији је потребан спољни извор енергије да би функционисао. батерија је повезана са обе електроде које покрећу рад електролитичке ћелије. | Галванска или волтачка ћелија не захтева никакав спољни извор енергије јер производи своју енергију. |
| Пуњења | Електролитичка ћелија садржи негативно наелектрисане аноде и позитивно наелектрисане катоде. | Галванска ћелија или волтаична ћелија садржи позитивно наелектрисану аноду и негативно наелектрисане катоде. |
| Реакције | Електролитичке ћелије користе спонтане реакције за производњу хемијске енергије. Конвертује електричну енергију у хемијску. | Галванске или волтаичне ћелије користе неспонтанереакције за производњу електричне енергије. претвара хемијску енергију у електричну енергију потребну за рад. |
Разлике између галванске и електролитичке ћелије
Практичне примене електролитичке ћелије
Електролитичка ћелија је направио важну улогу за себе у данашњем друштву и користи се у масовном броју. Практичност и значај електролитичких ћелија су наведени у наставку:
- Користи се за припрему металног натријума из растопљеног натријум хлорида помоћу довнс ћелије.
- Користи се за добијање гасова хлора и припрему каустичне соде (НаОХ) из воденог раствора натријум хлорида помоћу Нелсон ћелије.
- Користи се за екстракцију металног алуминијума.
- Користи се у електро-рафинацији бакра.
- Електролитичке ћелије се користе за галванизацију метала.
- Електролитичка ћелија се користи за производњу гаса кисеоника и водоника из воде испоруком путем електролизе.
Практичне примене галванске или напонске Ћелије
Галванске или волтаичне ћелије су важан изум за данашњи свет и човечанство их користи надалеко. Електрична енергија је основна потреба савременог живота и њена производња је један од најтежих процеса, али имамо толико начина да произведемо електричну енергију.
Галванске или волтаичне ћелије су једна од најранијих метода за производњу електричне енергије. Још увекима значајан значај међу новим и савременим методама производње електричне енергије.
- Процес галванских ћелија има много типова и утиче на људски живот на много начина. Суве ћелије или батерије, које обично користимо у свакодневном животу, напајају наше батеријске лампе, ТВ контроле, контролере за игре и многе друге ствари.
- Оловна батерија је такође свакодневни пример галванске ћелије. Функција оловне батерије је да производи електричну енергију када је главно напајање искључено. Обично се користи као резервна копија у кућама и на радним местима.
- Горивне ћелије се широко користе у индустрији јер њихова резервна копија мора бити већа. Они се користе када нема струје и машине морају да раде.
Галванска ћелија наспрам електролитичке ћелије
Закључак
- Да сумирамо горе, и електролитичке и галванске или волтаичне ћелије имају свој значај у овом савременом свету по свом јединственом начину обраде. Обе ове ћелије су још увек у употреби и још увек служе својој сврси.
- Све у свему, метод који се подвргава производњи и електролитских и галванских ћелија је једноставан и лако доступан обичном човеку.
- Електролитичка ћелија не може да ради када није повезана ни са једним спољним напајањем. Насупрот томе, галванска колекција нема потребе да буде повезана на било које спољно напајање док производисопствену моћ.
- Употреба обе ћелије је сада позната и позната у целом свету, а овај изузетан изум сада је део наставног плана и програма младих и учи се сваком детету у данашње време.

