តើអ្វីជាភាពខុសគ្នារវាងកោសិកាអេឡិចត្រូលីត និងកោសិកាកាល់វ៉ានីក? (ការវិភាគលម្អិត) - ភាពខុសគ្នាទាំងអស់។

តារាងមាតិកា
វិទ្យាសាស្ត្របានធ្វើអព្ភូតហេតុជាច្រើននៅក្នុងអតីតកាល ហើយពិភពលោកកំពុងធ្វើក្នុងពេលបច្ចុប្បន្ន ហើយកំពុងត្រៀមខ្លួនសម្រាប់អនាគត។ ពាក្យ "វិទ្យាសាស្រ្ត" ត្រូវបានគេយកចេញពីពាក្យឡាតាំង "Scientia" ដែលមានន័យថាចំណេះដឹង។ ចំណេះដឹងនេះគឺផ្អែកលើសម្មតិកម្ម ការសង្កេត និងការពិសោធន៍នៃវិទ្យាសាស្ត្រសកល។
ដូចនៅក្នុងគីមីវិទ្យា ចលនានៃអ៊ីយ៉ុងត្រូវបានពិភាក្សា ដែលទាមទារប្រភេទកោសិកាផ្សេងៗគ្នា។ ឧបករណ៍ដែលបំលែងថាមពលគីមីទៅជាថាមពលអគ្គិសនី ឬផ្ទុយមកវិញដោយប្រតិកម្ម redox ត្រូវបានគេស្គាល់ថាជាកោសិកាអេឡិចត្រូគីមី។ កោសិកាអេឡិចត្រូគីមីគឺអេឡិចត្រូលីតនិងកាល់វ៉ានីក (កោសិកាវ៉ុលតាក) ។
កោសិកាអេឡិចត្រូលីតគឺជាកោសិកាដែលមានប៉ូលវិជ្ជមាន និងអវិជ្ជមានដែលគេស្គាល់ថាជា anode និង cathode ។ ម្យ៉ាងវិញទៀត កោសិកាកាល់វ៉ានីកត្រូវបានកំណត់ថាជាកោសិកាអេឡិចត្រូគីមីដែលត្រូវបានប្រើដើម្បីបំប្លែងថាមពលគីមីនៃប្រតិកម្ម redox ដោយឯកឯងទៅជាថាមពលអគ្គិសនី។
កោសិកាអេឡិចត្រូលីតត្រូវបានប្រើសម្រាប់ដំណើរការនៃអេឡិចត្រូលីត។ ដែលជាដំណើរការនៃចរន្តឆ្លងកាត់អេឡិចត្រូលីត។ ដោយសារតែនេះការធ្វើចំណាកស្រុកនៃអ៊ីយ៉ុងអវិជ្ជមាននិងវិជ្ជមានឆ្ពោះទៅរក anode និង cathode កើតឡើង។
កោសិកាកាល់វ៉ានីក ហៅផងដែរថា កោសិកាវ៉ុលតាអ៊ីក គឺជាកោសិកាអេឡិចត្រូគីមី ដែលប្រើប្រតិកម្មគីមីដើម្បីបង្កើតថាមពលអគ្គិសនី។
កោសិកាទាំងពីរនេះនៅតែមានប្រយោជន៍ដូចកាលដែលពួកវាមាននៅពេលបង្កើត ដែលមានន័យថាពួកគេមិនបាត់បង់តម្លៃរបស់ពួកគេទេ។នៅក្នុងសង្គមបដិវត្តន៍សព្វថ្ងៃ។
សារៈសំខាន់ និងភាពខុសគ្នារវាងកោសិកា galvanic ឬកោសិកាវ៉ុលតាក និងកោសិកាអេឡិចត្រូលីតត្រូវបានពិភាក្សាយ៉ាងទូលំទូលាយនៅក្នុងអត្ថបទនេះ។
កោសិកាអេឡិចត្រូលីក៖ តើវាដំណើរការយ៉ាងដូចម្តេច?
ឧបករណ៍អេឡិចត្រូលីតដែលប្រើថាមពលអគ្គិសនីដើម្បីជំរុញឱ្យមានប្រតិកម្ម redox ដែលមិនកើតឡើងដោយឯកឯង ត្រូវបានគេស្គាល់ថាជាកោសិកាអេឡិចត្រូលីត។ សារធាតុគីមីមួយចំនួនអាចត្រូវបាន electrolyzed ដោយប្រើកោសិកា electrolytic ដែលបន្ទាប់មកត្រូវបានគេហៅថា electrochemical cell ។

កោសិកាអេឡិចត្រូលីត និងកុងទ័រ
ឧទាហរណ៍ ទឹកអាចត្រូវបានអេឡិចត្រូលីសដើម្បីបង្កើតឧស្ម័នអុកស៊ីហ្សែន និងអ៊ីដ្រូសែនឧស្ម័នដោយប្រើកោសិកាអេឡិចត្រូលីត។ នេះត្រូវបានសម្រេចដោយការប្រើប្រាស់លំហូរនៃអេឡិចត្រុង (ទៅក្នុងបរិយាកាសប្រតិកម្ម) ដើម្បីបំបែករបាំងថាមពលធ្វើឱ្យសកម្មរបស់ប្រតិកម្ម redox ដែលមិនកើតឡើងដោយឯកឯង។
ផ្នែកសំខាន់ៗនៃកោសិកាអេឡិចត្រូលីតគឺ៖
- cathode (បន្ទុកអវិជ្ជមាន)
- anode (បន្ទុកវិជ្ជមាន)
- អេឡិចត្រូលីតមួយ
អ៊ីយ៉ុងវិជ្ជមានដែលបំបែកនៅក្នុងអេឡិចត្រូលីតត្រូវបានទាញទៅ cathode នៃ កោសិកាអេឡិចត្រូលីតនៅពេលដែលចរន្តអគ្គិសនីខាងក្រៅហូរកាត់វា។ នេះបណ្តាលឱ្យអ៊ីយ៉ុងដែលមានបន្ទុកវិជ្ជមានទៅតាំងលំនៅនៅលើ cathode ។
អាណូតដែលមានបន្ទុកវិជ្ជមានត្រូវបានទៅជិតដោយអ៊ីយ៉ុងដែលមានបន្ទុកអវិជ្ជមានក្នុងពេលតែមួយ។
តើអ្វីទៅជាកោសិកា Galvanic ហើយវាដំណើរការដោយរបៀបណា?
ក្រឡា galvanic ឬ voltaic គឺជាឧបករណ៍ដែលបំប្លែងថាមពលគីមី ទៅជាថាមពលអគ្គិសនី តាមរយៈប្រតិកម្ម redox ចៃដន្យ។ ក្រឡាកាល់វ៉ានីកគឺជាឧបករណ៍គីមីអេឡិចត្រូនិចដែលបង្កើតចរន្តអគ្គិសនីតាមរយៈប្រតិបត្តិការគីមី។
ឧបករណ៍ទូទៅមានអេឡិចត្រូតពីរផ្សេងគ្នា។
មួយគឺធ្វើពីទង់ដែង ហើយមួយទៀតគឺស័ង្កសី។ ទាំងពីរត្រូវបានដាក់ក្នុង beakers ដាច់ដោយឡែកដែលមានអ៊ីយ៉ុងដែករៀងៗខ្លួននៅក្នុងដំណោះស្រាយ ដែលត្រូវបានតភ្ជាប់ដោយស្ពានអំបិល និងត្រូវបានបំបែកដោយភ្នាស porous ។
គោលបំណងនៃការបង្កើតកោសិកាអេឡិចត្រូលីតគឺដើម្បីបំប្លែងថាមពលអគ្គិសនីទៅជាថាមពលគីមី ដោយបញ្ចេញអេឡិចត្រូលីតទៅជាលោហៈពីរដែលគិតថ្លៃ និងភ្ជាប់ទៅនឹងថ្មរៀងៗខ្លួន។
មូលហេតុនៃការផលិត កោសិកា galvanic ឬ voltaic cells គឺថាពួកវាមានសមត្ថភាពបំប្លែងថាមពលគីមីទៅជាថាមពលអគ្គិសនី ដែលត្រូវការសម្រាប់គោលបំណងការងារ។
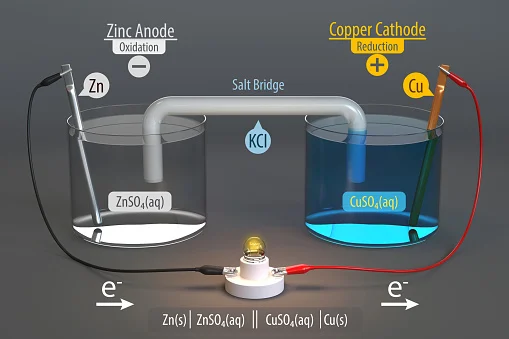
ការពិសោធន៍កោសិកា Galvanic
ការបែងចែកការពិតរវាងកោសិកា Galvanic និង Electrolytic
កោសិកាអេឡិចត្រូលីត និងកោសិកាកាល់វ៉ានីកមានលក្ខណៈផ្ទុយគ្នាមួយចំនួនដែលត្រូវបានពិភាក្សានៅក្នុងតារាងខាងក្រោម។
សូមមើលផងដែរ: តើអ្វីជាភាពខុសគ្នាសំខាន់រវាង "Buenas" និង "Buenos" នៅក្នុងភាសាអេស្ប៉ាញ? (បង្ហាញ) - ភាពខុសគ្នាទាំងអស់។| លក្ខណៈពិសេស | កោសិកាអេឡិចត្រូលីក <19 | កោសិកា Galvanic ឬ Voltaic | |
|---|---|---|---|
| ផលិតកម្ម | កោសិកាអេឡិចត្រូលីតប្រើនាវាដែលពោរពេញទៅដោយអេឡិចត្រូលីត ហើយមានអេឡិចត្រូតពីរបានជ្រលក់ក្នុងវាដែលត្រូវបានភ្ជាប់ទៅនឹងថ្មរៀងៗខ្លួនដែលធ្វើឱ្យពួកវាមានអាណូត និងcathode។ | កោសិកា galvanic ឬ voltaic cell ត្រូវបានផលិតនៅពេលដែល beakers ពីរពោរពេញទៅដោយ electrolytes និង electrodes ពីរត្រូវបានជ្រលក់ក្នុងដំណោះស្រាយនេះ។ ចំពុះទាំងនេះត្រូវបានតភ្ជាប់ដោយស្ពានអំបិល ហើយអេឡិចត្រូតទាំងពីរត្រូវបានតភ្ជាប់ដោយថ្មរៀងៗខ្លួន។ ថាមពលគីមីតាមរយៈប្រតិកម្ម redox ដែលកើតឡើងដោយឯកឯង និងទទួលខុសត្រូវលើការផលិតថាមពលអគ្គិសនី។ | កោសិកា galvanic ឬ voltaic គឺជាកោសិកាដែលបំលែងថាមពលគីមីទៅជាថាមពលអគ្គិសនីតាមរយៈប្រតិកម្ម redox ដែលមានប្រយោជន៍ខ្លាំងណាស់សម្រាប់ គោលបំណងការងារ។ |
| ប្រភពថាមពល | កោសិកាអេឡិចត្រូលីតត្រូវការប្រភពថាមពលខាងក្រៅដើម្បីដំណើរការ។ ថ្មមួយត្រូវបានភ្ជាប់ទៅអេឡិចត្រូតទាំងពីរដែលចាប់ផ្តើមដំណើរការនៃកោសិកាអេឡិចត្រូលីត។ | កោសិកា galvanic ឬ voltaic មិនតម្រូវឱ្យមានប្រភពថាមពលខាងក្រៅណាមួយទេ ដោយសារវាផលិតថាមពលរបស់វា។ | |
| ការគិតថ្លៃ | កោសិកាអេឡិចត្រូលីតមានផ្ទុក anodes ចោទប្រកាន់អវិជ្ជមាន និង cathodes សាកវិជ្ជមាន។ | កោសិកា Galvanic ឬ voltaic cell មាន anode សាកវិជ្ជមាន និង cathodes សាកអវិជ្ជមាន។<19 | |
| ប្រតិកម្ម | កោសិកាអេឡិចត្រូលីតប្រើប្រតិកម្មដោយឯកឯងដើម្បីផលិតថាមពលគីមី។ វាបំប្លែងថាមពលអគ្គិសនីទៅជាថាមពលគីមី។ | កោសិកា Galvanic ឬ voltaic ប្រើដោយឯកឯងប្រតិកម្មដើម្បីផលិតថាមពលអគ្គិសនី។ វាបំប្លែងថាមពលគីមីទៅជាថាមពលអគ្គិសនីដែលត្រូវការសម្រាប់ការងារ។ |
ភាពខុសគ្នារវាងកោសិកា Galvanic និង Electrolytic
ការអនុវត្តជាក់ស្តែងនៃកោសិកាអេឡិចត្រូលីត
កោសិកាអេឡិចត្រូលីត បានដើរតួយ៉ាងសំខាន់សម្រាប់ខ្លួនវានៅក្នុងសង្គមបច្ចុប្បន្ន ហើយត្រូវបានប្រើប្រាស់ជាចំនួនច្រើន។ ភាពជាក់ស្តែង និងសារៈសំខាន់នៃកោសិកាអេឡិចត្រូលីតត្រូវបានរាយខាងក្រោម៖
- វាត្រូវបានប្រើដើម្បីរៀបចំដែកសូដ្យូមពីក្លរួសូដ្យូមរលាយដោយប្រើកោសិកាចុះក្រោម។
- វាត្រូវបាន ប្រើដើម្បីទទួលបានក្លរីនហ្គា s និងរៀបចំសូដាដុត (NaOH) ពីក្លរួសូដ្យូមក្នុងទឹកដោយកោសិកាណិលសុន។
- វាត្រូវបានប្រើដើម្បីទាញយកលោហៈអាលុយមីញ៉ូម។
- វាត្រូវបានប្រើនៅក្នុងការចម្រាញ់អេឡិចត្រូលីតនៃទង់ដែង។
- កោសិកាអេឡិចត្រូលីតត្រូវបានប្រើសម្រាប់ការផ្លាតលោហធាតុ។
- កោសិកាអេឡិចត្រូលីតត្រូវបានប្រើដើម្បីផលិតឧស្ម័នអុកស៊ីហ្សែន និងឧស្ម័នអ៊ីដ្រូសែនពីទឹក ដោយបញ្ជូនវាតាមរយៈអេឡិចត្រូលីស។
ការអនុវត្តជាក់ស្តែងនៃហ្គាវ៉ានីក ឬវ៉ុលតាអ៊ីក កោសិកា
កោសិកា Galvanic ឬ voltaic គឺជាការច្នៃប្រឌិតដ៏សំខាន់សម្រាប់ពិភពលោកបច្ចុប្បន្ន ហើយត្រូវបានប្រើប្រាស់យ៉ាងទូលំទូលាយដោយមនុស្សជាតិ។ អគ្គិសនីគឺជាតម្រូវការមូលដ្ឋាននៃជីវិតសម័យទំនើប ហើយការផលិតរបស់វាគឺជាដំណើរការដ៏លំបាកបំផុតមួយ ប៉ុន្តែយើងមានវិធីជាច្រើនដើម្បីផលិតអគ្គិសនី។
កោសិកា Galvanic ឬ voltaic គឺជាវិធីសាស្រ្តដំបូងបំផុតមួយនៃការបង្កើតអគ្គិសនី។ វានៅតែមានសារៈសំខាន់យ៉ាងសំខាន់ក្នុងចំណោមវិធីសាស្រ្តថ្មី និងទំនើបនៃការផលិតអគ្គិសនី។
សូមមើលផងដែរ: A Quarter Pounder Vs. Whopper Showdown រវាង McDonald's និង Burger King (លម្អិត) - ភាពខុសគ្នាទាំងអស់- ដំណើរការនៃកោសិកា galvanic មានច្រើនប្រភេទ ហើយប៉ះពាល់ដល់ជីវិតមនុស្សតាមវិធីជាច្រើន។ កោសិកាស្ងួត ឬថ្មដែលយើងប្រើជាទូទៅក្នុងជីវិតប្រចាំថ្ងៃរបស់យើង ផ្តល់ថាមពលដល់ភ្លើងពិល ការគ្រប់គ្រងទូរទស្សន៍ ឧបករណ៍បញ្ជាហ្គេម និងរបស់ជាច្រើនទៀត។
- ថ្មផ្ទុកថាមពលក៏ជា ឧទាហរណ៍ប្រចាំថ្ងៃនៃកោសិកា galvanic ។ មុខងាររបស់ថ្មផ្ទុកនាំមុខគឺបង្កើតចរន្តអគ្គិសនីនៅពេលការផ្គត់ផ្គង់ថាមពលចម្បងបិទ។ វាត្រូវបានគេប្រើជាទូទៅក្នុងការបម្រុងទុកនៅក្នុងផ្ទះ និងកន្លែងធ្វើការ។
- កោសិកាឥន្ធនៈត្រូវបានប្រើប្រាស់យ៉ាងទូលំទូលាយនៅក្នុងឧស្សាហកម្ម ដោយសារការបម្រុងទុករបស់ពួកវាត្រូវការធំជាង។ ទាំងនេះត្រូវបានប្រើប្រាស់នៅពេលដែលអគ្គិសនីរលត់ ហើយម៉ាស៊ីនត្រូវដំណើរការ។
កោសិកា Galvanic ធៀបនឹងកោសិកាអេឡិចត្រូលីត
សេចក្តីសន្និដ្ឋាន
- សរុបមក វាឡើង ទាំងកោសិកាអេឡិចត្រូលីត និងកាល់វ៉ានីក ឬវ៉ុលតាអ៊ីក មានសារៈសំខាន់ផ្ទាល់របស់ពួកគេនៅក្នុងពិភពទំនើបនេះ ក្នុងវិធីកែច្នៃតែមួយគត់របស់ពួកគេ។ កោសិកាទាំងពីរនេះនៅតែត្រូវបានប្រើប្រាស់ ហើយនៅតែបម្រើគោលបំណងរបស់ពួកគេ។
- ជារួម វិធីសាស្ត្រដែលឆ្លងកាត់ការផលិតកោសិកាអេឡិចត្រូលីត និងកាល់វ៉ានីកគឺសាមញ្ញ និងងាយស្រួលសម្រាប់មនុស្សទូទៅ។
- កោសិកាអេឡិចត្រូលីតមិនអាចដំណើរការបានទេ នៅពេលដែលវាមិនភ្ជាប់ទៅការផ្គត់ផ្គង់ថាមពលខាងក្រៅណាមួយឡើយ។ ផ្ទុយទៅវិញការប្រមូលផ្តុំ galvanic មិនចាំបាច់ត្រូវបានភ្ជាប់ទៅនឹងការផ្គត់ផ្គង់ថាមពលខាងក្រៅណាមួយដូចដែលវាផលិតអំណាចរបស់ខ្លួន។
- ការប្រើប្រាស់កោសិកាទាំងពីរឥឡូវនេះមានភាពល្បីល្បាញ និងធ្លាប់ស្គាល់នៅក្នុងពិភពលោកទាំងមូល ហើយការច្នៃប្រឌិតដ៏អស្ចារ្យនេះឥឡូវនេះជាផ្នែកមួយនៃកម្មវិធីសិក្សារបស់យុវជន ហើយត្រូវបានបង្រៀនដល់កុមារគ្រប់រូបនាពេលបច្ចុប្បន្ននេះ។

