ຄວາມແຕກຕ່າງລະຫວ່າງຈຸລັງໄຟຟ້າ ແລະເຊລ Galvanic ແມ່ນຫຍັງ? (ການວິເຄາະລະອຽດ) – ຄວາມແຕກຕ່າງທັງຫມົດ

ສາລະບານ
ວິທະຍາສາດໄດ້ເຮັດສິ່ງມະຫັດສະຈັນຫຼາຍຢ່າງໃນອະດີດ, ແລະໂລກກຳລັງເຮັດໃນປະຈຸບັນ ແລະກຽມພ້ອມສຳລັບອະນາຄົດ. ຄໍາວ່າ "ວິທະຍາສາດ" ໄດ້ມາຈາກຄໍານາມ "ວິທະຍາສາດ", ຊຶ່ງຫມາຍຄວາມວ່າຄວາມຮູ້; ຄວາມຮູ້ນີ້ແມ່ນອີງໃສ່ສົມມຸດຕິຖານ, ການສັງເກດການ, ແລະການທົດລອງຂອງວິທະຍາສາດທົ່ວໄປ.
ເບິ່ງ_ນຳ: ຄວາມແຕກຕ່າງລະຫວ່າງດາບຍາວ ແລະດາບສັ້ນແມ່ນຫຍັງ? (ສົມທຽບ) – ຄວາມແຕກຕ່າງທັງຫມົດໃນດ້ານເຄມີສາດ, ການເຄື່ອນໄຫວຂອງ ion ແມ່ນໄດ້ຖືກອະທິບາຍ, ເຊິ່ງຮຽກຮ້ອງໃຫ້ມີປະເພດຕ່າງໆຂອງເຊລ. ອຸປະກອນທີ່ປ່ຽນພະລັງງານເຄມີເປັນພະລັງງານໄຟຟ້າຫຼືໃນທາງກັບກັນໂດຍການປະຕິກິລິຢາ redox ເປັນທີ່ຮູ້ຈັກເປັນເຊນ electrochemical. ຈຸລັງ electrochemical ແມ່ນ electrolytic ແລະ galvanic (ຈຸລັງ voltaic).
ເບິ່ງ_ນຳ: ຄວາມແຕກຕ່າງລະຫວ່າງຊັອກເກັດ CPU FAN, ເຕົ້າຮັບ CPU OPT, ແລະຊັອກເກັດ SYS FAN ໃນເມນບອດແມ່ນຫຍັງ? - ຄວາມແຕກຕ່າງທັງຫມົດເຊລ electrolytic ແມ່ນເຊລທີ່ປະກອບດ້ວຍຂົ້ວບວກ ແລະລົບ ທີ່ເອີ້ນວ່າ anode ແລະ cathode. ໃນທາງກົງກັນຂ້າມ, ເຊນ galvanic ຖືກກໍານົດເປັນຈຸລັງໄຟຟ້າທີ່ໃຊ້ໃນການປ່ຽນພະລັງງານເຄມີຂອງປະຕິກິລິຍາ redox spontaneous ເປັນພະລັງງານໄຟຟ້າ.
ຈຸລັງ electrolytic ແມ່ນໃຊ້ສໍາລັບຂະບວນການຂອງ electrolysis, ເຊິ່ງເປັນຂະບວນການຂອງກະແສໄຟຟ້າຜ່ານ electrolyte. ດ້ວຍເຫດຜົນນີ້, ການເຄື່ອນຍ້າຍຂອງ ions ລົບແລະບວກໄປສູ່ anode ແລະ cathode ເກີດຂື້ນ.
ເຊລ galvanic, ເຊິ່ງເອີ້ນກັນວ່າ ເຊລ voltaic, ແມ່ນເຊນໄຟຟ້າເຄມີທີ່ໃຊ້ປະຕິກິລິຍາເຄມີເພື່ອສ້າງພະລັງງານໄຟຟ້າ.
ທັງສອງເຊລເຫຼົ່ານີ້ຍັງມີປະໂຫຍດຄືກັບຕອນທີ່ພວກມັນປະດິດສ້າງ, ຊຶ່ງໝາຍຄວາມວ່າພວກມັນບໍ່ໄດ້ສູນເສຍຄຸນຄ່າຂອງມັນ.ໃນສັງຄົມປະຕິວັດໃນປັດຈຸບັນ.
ຄວາມສຳຄັນ ແລະຄວາມແຕກຕ່າງລະຫວ່າງເຊລ galvanic, ຫຼື cell voltaic, ແລະ electrolytic cells ໄດ້ຖືກພິຈາລະນາຢ່າງກວ້າງຂວາງໃນບົດຄວາມນີ້.
Electrolytic Cell: ມັນເຮັດວຽກແນວໃດ?
ອຸປະກອນ electrolytic ທີ່ໃຊ້ພະລັງງານໄຟຟ້າເພື່ອກະຕຸ້ນປະຕິກິລິຍາ redox ທີ່ບໍ່ເປັນຕົວຕົນແມ່ນຮູ້ຈັກເປັນເຊລ electrolytic. ສານເຄມີບາງຊະນິດສາມາດຖືກ electrolyzed ໂດຍໃຊ້ຈຸລັງ electrolytic, ເຊິ່ງຫຼັງຈາກນັ້ນເອີ້ນວ່າຈຸລັງ electrochemical.

ຈຸລັງໄຟຟ້າ ແລະຕົວເກັບປະຈຸ
ຕົວຢ່າງເຊັ່ນ, ນໍ້າສາມາດຖືກ electrolyzed ເພື່ອສ້າງອາຍແກັສອອກຊິເຈນ ແລະ hydrogen ອາຍແກັສດ້ວຍການໃຊ້ເຊລ electrolytic. ອັນນີ້ແມ່ນເຮັດໄດ້ໂດຍການໃຊ້ການໄຫຼຂອງອິເລັກຕອນ (ເຂົ້າໄປໃນສະພາບແວດລ້ອມຕິກິຣິຍາ) ເພື່ອທໍາລາຍອຸປະສັກພະລັງງານການກະຕຸ້ນຂອງປະຕິກິລິຢາ redox ທີ່ບໍ່ແມ່ນ spontaneous.
ພາກສ່ວນຕົ້ນຕໍຂອງຈຸລັງໄຟຟ້າແມ່ນ:
- a cathode (ຄ່າລົບ)
- Anode (ຄ່າບວກ)
- A electrolyte
Ion ບວກທີ່ແຍກຕົວອອກໃນ electrolyte ຖືກດຶງໄປຫາ cathode ຂອງ ຈຸລັງ electrolytic ເມື່ອກະແສໄຟຟ້າພາຍນອກໄຫຼຜ່ານມັນ. ອັນນີ້ເຮັດໃຫ້ໄອອອນທີ່ຖືກຄິດຄ່າບວກຕັ້ງຢູ່ໃນ cathode.
ອະໂນດທີ່ມີສາກບວກແມ່ນເຂົ້າໄປຫາ ion ທີ່ມີຄ່າລົບໃນເວລາດຽວກັນ.
ເຊລ Galvanic ແມ່ນຫຍັງ ແລະມັນເຮັດວຽກແນວໃດ?
ເຊລ galvanic ຫຼື voltaic ເປັນອຸປະກອນທີ່ແປງພະລັງງານເຄມີ ເປັນພະລັງງານໄຟຟ້າ ໂດຍຜ່ານປະຕິກິລິຍາ redox ແບບສຸ່ມ. ເຊລ galvanic ເປັນອຸປະກອນໄຟຟ້າເຄມີທີ່ສ້າງໄຟຟ້າໂດຍຜ່ານການປະຕິບັດທາງເຄມີ.
ອຸປະກອນທົ່ວໄປປະກອບດ້ວຍສອງ electrodes ທີ່ແຕກຕ່າງກັນ.
ອັນໜຶ່ງເຮັດດ້ວຍທອງແດງ ແລະ ອີກອັນໜຶ່ງແມ່ນສັງກະສີ; ທັງສອງແມ່ນຖືກຈັດໃສ່ໃນ beakers ແຍກຕ່າງຫາກທີ່ມີ ions ໂລຫະຂອງເຂົາເຈົ້າໃນການແກ້ໄຂ, ເຊິ່ງເຊື່ອມຕໍ່ໂດຍຂົວເກືອແລະຖືກແຍກອອກໂດຍເຍື່ອ porous.
ຈຸດປະສົງຂອງການຜະລິດເຊລ electrolytic ແມ່ນເພື່ອປ່ຽນພະລັງງານໄຟຟ້າເປັນພະລັງງານເຄມີໂດຍການເປີດເຜີຍ electrolyte ໃຫ້ກັບໂລຫະສອງຢ່າງທີ່ຄິດຄ່າແລະເຊື່ອມຕໍ່ກັບຫມໍ້ໄຟ, ຕາມລໍາດັບ.
ສາເຫດຂອງການຜະລິດຂອງ ຈຸລັງ galvanic ຫຼື voltaic cell ແມ່ນວ່າພວກມັນສາມາດປ່ຽນພະລັງງານເຄມີເປັນພະລັງງານໄຟຟ້າ, ເຊິ່ງຕ້ອງການສໍາລັບການເຮັດວຽກ.
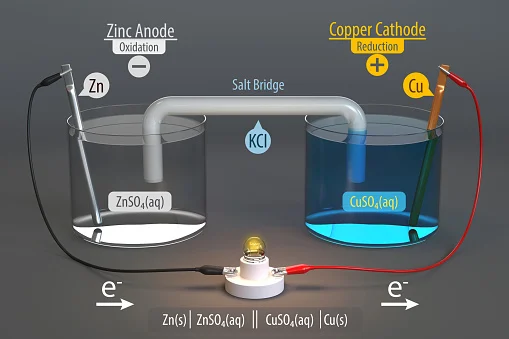
Galvanic Cell Experiment
ການຈໍາແນກຂໍ້ເທັດຈິງລະຫວ່າງ Galvanic ແລະ Electrolytic Cells
ເຊລໄຟຟ້າ ແລະເຊລກວານິກມີຄຸນສົມບັດທີ່ກົງກັນຂ້າມກັນໃນຕາຕະລາງຂ້າງລຸ່ມນີ້.
| ຄຸນສົມບັດ | ຈຸລັງໄຟຟ້າ <19 | ເຊລ Galvanic ຫຼື Voltaic |
|---|---|---|
| ການຜະລິດ | ເຊລ electrolytic ໃຊ້ເຮືອທີ່ເຕັມໄປດ້ວຍ electrolytes ແລະມີສອງ electrodes dipped ໃນມັນທີ່ເຊື່ອມຕໍ່ກັບຫມໍ້ໄຟຕາມລໍາດັບເຮັດໃຫ້ພວກເຂົາ anode ແລະcathode. | ເຊລ galvanic ຫຼື voltaic cell ແມ່ນຜະລິດເມື່ອ beakers ສອງອັນເຕັມໄປດ້ວຍ electrolytes ແລະ electrodes ສອງໄດ້ຖືກຈຸ່ມຢູ່ໃນການແກ້ໄຂນີ້. ເບກເກີເຫຼົ່ານີ້ຖືກເຊື່ອມຕໍ່ໂດຍຂົວເກືອ ແລະທັງສອງ electrodes ແມ່ນເຊື່ອມຕໍ່ໂດຍຫມໍ້ໄຟຕາມລໍາດັບ. |
| ພະລັງງານ | ເຊລ electrolytic ປ່ຽນພະລັງງານໄຟຟ້າເປັນ ພະລັງງານເຄມີໂດຍຜ່ານປະຕິກິລິຢາ redox ທີ່ເປັນ spontaneous ແລະຮັບຜິດຊອບການຜະລິດພະລັງງານໄຟຟ້າ. | ເຊລ galvanic ຫຼື voltaic ເປັນຈຸລັງທີ່ປ່ຽນພະລັງງານເຄມີເປັນພະລັງງານໄຟຟ້າໂດຍຜ່ານປະຕິກິລິຍາ redox ທີ່ມີປະໂຫຍດຫຼາຍສໍາລັບ ຈຸດປະສົງໃນການເຮັດວຽກ. |
| ແຫຼ່ງພະລັງງານ | ເຊລ electrolytic ຕ້ອງການແຫຼ່ງພະລັງງານພາຍນອກເພື່ອເຮັດວຽກ. ແບດເຕີຣີແມ່ນເຊື່ອມຕໍ່ກັບທັງສອງ electrodes ທີ່ເລີ່ມຕົ້ນການເຮັດວຽກຂອງເຊນໄຟຟ້າ. | ເຊລ galvanic ຫຼື voltaic ບໍ່ຕ້ອງການແຫຼ່ງພະລັງງານຈາກພາຍນອກຍ້ອນວ່າມັນຜະລິດພະລັງງານຂອງມັນ. |
| ສາກໄຟ | ເຊລ electrolytic ມີ anodes ມີສາກລົບ ແລະ cathodes ທີ່ມີສາກບວກ. | ເຊລ Galvanic ຫຼື voltaic cell ປະກອບມີ anode ມີສາກບວກ ແລະ cathodes ທີ່ມີສາກລົບ.<19 |
| ປະຕິກິລິຍາ | ຈຸລັງໄຟຟ້າໃຊ້ປະຕິກິລິຍາ spontaneous ເພື່ອຜະລິດພະລັງງານເຄມີ. ມັນປ່ຽນພະລັງງານໄຟຟ້າເປັນພະລັງງານເຄມີ. | ເຊລ Galvanic ຫຼື voltaic ໃຊ້ທີ່ບໍ່ແມ່ນ spontaneousປະຕິກິລິຍາເພື່ອຜະລິດພະລັງງານໄຟຟ້າ. ມັນປ່ຽນພະລັງງານເຄມີໄປເປັນພະລັງງານໄຟຟ້າທີ່ຕ້ອງການສໍາລັບການເຮັດວຽກ. ໄດ້ມີບົດບາດສໍາຄັນສໍາລັບຕົວມັນເອງໃນສັງຄົມປະຈຸບັນແລະຖືກນໍາໃຊ້ໃນຈໍານວນມະຫາຊົນ. ການປະຕິບັດ ແລະ ຄວາມສຳຄັນຂອງເຊລ electrolytic ແມ່ນລະບຸໄວ້ຂ້າງລຸ່ມນີ້:
ການປະຕິບັດຕົວຈິງຂອງ Galvanic ຫຼື Voltaic ເຊລເຊລ Galvanic ຫຼື voltaic ເປັນສິ່ງປະດິດທີ່ສຳຄັນສຳລັບໂລກທຸກວັນນີ້ ແລະ ມະນຸດຊາດຖືກນຳໃຊ້ໄປໄກ ແລະ ກວ້າງຂວາງ. ໄຟຟ້າແມ່ນມີຄວາມຈໍາເປັນພື້ນຖານຂອງຊີວິດທີ່ທັນສະໄຫມແລະການຜະລິດຂອງມັນແມ່ນຫນຶ່ງໃນຂະບວນການທີ່ຫຍຸ້ງຍາກທີ່ສຸດ, ແຕ່ພວກເຮົາມີຫຼາຍວິທີທີ່ຈະຜະລິດໄຟຟ້າ. ເຊລ Galvanic ຫຼື voltaic ແມ່ນໜຶ່ງໃນວິທີການຜະລິດກະແສໄຟຟ້າໃນໄວທີ່ສຸດ. ຍັງມີຄວາມສຳຄັນທີ່ສຳຄັນໃນບັນດາວິທີຜະລິດໄຟຟ້າແບບໃໝ່ ແລະ ທັນສະໄໝ.
ເຊລ Galvanic ທຽບກັບຈຸລັງໄຟຟ້າ ສະຫຼຸບ
|

