Electrolytic Cells ۽ Galvanic Cells جي وچ ۾ ڇا فرق آهي؟ (تفصيلي تجزيو) - سڀ فرق

مواد جي جدول
سائنس ماضي ۾ ڪيترائي عجائب ڪيا آهن، ۽ دنيا حال ۾ ڪري رهي آهي ۽ مستقبل لاءِ تيار ٿي رهي آهي. لفظ ”سائنس“ لاطيني لفظ ”سائنسيا“ مان ورتو ويو آهي، جنهن جي معنيٰ آهي علم؛ هي علم عالمگير سائنس جي مفروضن، مشاهدن ۽ تجربن تي ٻڌل آهي.
جيئن ڪيميا ۾، آئنز جي حرڪت تي بحث ڪيو ويو آهي، جنهن لاءِ مختلف قسمن جي سيلن جي ضرورت هوندي آهي. اهو اوزار جيڪو ڪيميائي توانائي کي برقي توانائي ۾ تبديل ڪري ٿو يا ان جي برعڪس هڪ ريڊڪس ردعمل ذريعي هڪ اليڪٽرروڪيميڪل سيل طور سڃاتو وڃي ٿو. اليڪٽرروڪيميڪل سيلز الیکٹروليٽڪ ۽ گليوانڪ (وولٽيڪ سيلز) آهن.
هڪ اليڪٽرولائيٽڪ سيل هڪ سيل آهي جيڪو مثبت ۽ منفي قطبن تي مشتمل هوندو آهي جنهن کي اينوڊ ۽ ڪيٿوڊ چئبو آهي. ٻئي طرف، هڪ galvanic سيل جي وضاحت ڪئي وئي آهي هڪ اليڪٽررو ڪيميڪل سيل جي طور تي جيڪو استعمال ڪيو ويندو آهي ڪيميائي توانائي کي spontaneous redox رد عمل جي ڪيميائي توانائي کي برقي توانائي ۾ تبديل ڪرڻ لاءِ.
Electrolytic cell electrolysis جي عمل لاءِ استعمال ٿيندو آهي، جيڪو اليڪٽرولائٽ ذريعي ڪرنٽ گذرڻ جو عمل آهي. ان جي ڪري، منفي ۽ مثبت آئنز جي لڏپلاڻ انوڊ ۽ ڪيٿوڊ ڏانهن ٿيندي آهي.
هڪ ڪهڪشان سيل، جنهن کي وولٽڪ سيل به سڏيو وڃي ٿو، هڪ اليڪٽررو ڪيميڪل سيل آهي جيڪو ڪيميائي رد عملن کي استعمال ڪري بجلي پيدا ڪري ٿو.
اهي ٻئي سيل اڃا به اوترا ئي ڪارآمد آهن جيئن اهي پنهنجي ايجاد جي وقت هئا، جنهن جو مطلب آهي ته انهن پنهنجو قدر نه وڃايو آهي.اڄ جي انقلابي سماج ۾.
گليوانڪ سيلز، يا وولٽيڪ سيلز، ۽ اليڪٽرولائيڪ سيلز جي وچ ۾ اهميت ۽ فرق هن آرٽيڪل ۾ وسيع بحث ڪيو ويو آهي.
اليڪٽرولائيٽ سيل: اهو ڪيئن ڪم ڪندو آهي؟
هڪ اليڪٽرولائيٽڪ ڊيوائس جيڪو بجليءَ جي توانائي کي استعمال ڪري هڪ غير خودڪشي ريڊڪس رد عمل پيدا ڪري ٿو، ان کي اليڪٽرولائيٽڪ سيل طور سڃاتو وڃي ٿو. ڪجهه ڪيميائي اليڪٽرولائيز سيلز استعمال ڪندي اليڪٽرولائيز ٿي سگهن ٿيون، جن کي پوءِ اليڪٽررو ڪيميڪل سيلز چئجي ٿو.

Electrolytic Cells ۽ capacitors
مثال طور، پاڻيءَ کي اليڪٽرولائيز ڪري سگهجي ٿو ته جيئن گيسيس آڪسيجن ۽ گيسيس هائيڊروجن ٺاهي سگهجي. اهو مڪمل ڪيو ويو آهي اليڪٽران جي وهڪري کي (رد عمل واري ماحول ۾) کي ٽوڙڻ لاءِ غير خود ساخته ريڊڪس رد عمل جي فعال ٿيڻ واري توانائي جي رڪاوٽ کي ٽوڙڻ لاءِ> هڪ ڪيٿوڊ (منفي چارج)
اليڪٽرولائيٽ ۾ الڳ ٿيل مثبت آئنز ڪيٿوڊ ڏانهن ڇڪيا ويندا آهن. اليڪٽرولائيٽ سيل جڏهن ٻاهرئين برقي ڪرنٽ ان جي ذريعي وهندو آهي. اهو مثبت طور تي چارج ٿيل آئنز کي ڪيٿوڊ تي آباد ڪرڻ جو سبب بڻائيندو آهي.
مثبت طور تي چارج ٿيل انوڊ هڪ ئي وقت منفي طور تي چارج ٿيل آئنز سان رابطو ڪيو ويندو آهي.
گليوانڪ سيل ڇا آهي ۽ اهو ڪيئن ڪم ڪندو آهي؟
هڪ galvanic يا voltaic سيل هڪ ڊوائيس آهي جيڪو تبديل ڪري ٿوڪيميائي توانائي برقي توانائي ۾ بي ترتيب ريڊڪس ردعمل ذريعي. galvanic cell هڪ اليڪٽررو ڪيميڪل ڊيوائس آهي جيڪو ڪيميائي عملن ذريعي بجلي ٺاهي ٿو.
عام اپريٽس ٻن مختلف اليڪٽروڊس تي مشتمل آهي.
هڪ ٽامي جو ٺهيل آهي ۽ ٻيو زنڪ؛ ٻنهي کي الڳ الڳ بيڪرن ۾ رکيل هوندو آهي جنهن ۾ انهن جي لاڳاپيل ڌاتو آئن محلول ۾ هوندا آهن، جيڪي هڪ لوڻ جي پل سان ڳنڍيل هوندا آهن ۽ هڪ ٻرندڙ جھلي سان الڳ هوندا آهن.
ڏسو_ پڻ: ENFP بمقابله ENTP شخصيت (سڀ ڪجهه تفصيل سان بيان ڪيو ويو آهي) - سڀ فرقاليڪٽرولائيٽ سيلز جي پيداوار جو مقصد برقي توانائي کي ڪيميائي توانائي ۾ تبديل ڪرڻ آهي اليڪٽرولائٽ کي ٻن ڌاتون کي ظاهر ڪري چارج ٿيل ۽ بيٽري سان ڳنڍيل آهي.
جي پيداوار جو سبب galvanic Cells يا voltaic Cells اهو آهي ته اهي ڪيميائي توانائيءَ کي برقي توانائي ۾ تبديل ڪرڻ جي قابل هوندا آهن، جيڪا ڪم جي مقصدن لاءِ گهربل هوندي آهي.
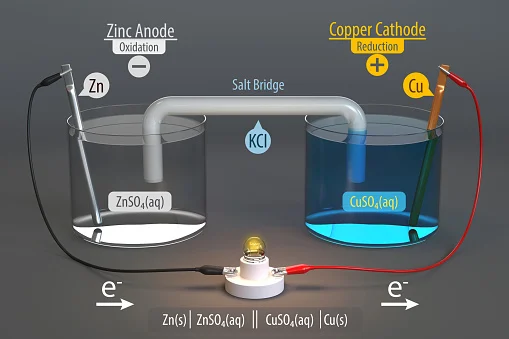
Galvanic Cell Experiment
Galvanic and Electrolytic Cells جي وچ ۾ فرق ڪندڙ حقيقتون
Electrolytic Cells ۽ galvanic cells ۾ ڪجھ متضاد خاصيتون آھن جن تي ھيٺ ڏنل جدول ۾ بحث ڪيو ويو آھي.
| خصوصيتون | اليڪٽرولائيٽڪ سيل <19 | Galvanic or Voltaic Cell |
|---|---|---|
| Production | Electrolytic cell هڪ برتن استعمال ڪندو آهي جيڪو اليڪٽرولائٽس سان ڀريل هوندو آهي ۽ ان ۾ ٻه اليڪٽروڊ ڊبل آهن جيڪي بيٽري سان ڳنڍيل آهن انهن کي اينوڊ ۽ڪيٿوڊ. | گليوانڪ سيل يا وولٽيڪ سيل تڏهن پيدا ٿيندو آهي جڏهن اليڪٽرولائٽس سان ڀريل ٻه بيڪر ۽ ٻه اليڪٽروڊ هن محلول ۾ ٻوڙي ويندا آهن. اهي بيڪر هڪ سالٽ پل سان جڙيل آهن ۽ ٻئي اليڪٽروڊز ترتيب سان هڪ بيٽري سان جڙيل آهن. |
| توانائي 17> | اليڪٽرولائيٽڪ سيل برقي توانائي ۾ تبديل ڪري ٿو. ڪيميائي توانائي هڪ ريڊ آڪس رد عمل جي ذريعي جيڪا spontaneous آهي ۽ برقي توانائي جي پيداوار جو انچارج آهي. | گليوانڪ يا وولٽائيڪ سيل هڪ سيل آهي جيڪو ڪيميائي توانائي کي برقي توانائي ۾ تبديل ڪري ٿو ريڊ آڪس رد عمل جي ذريعي جيڪو تمام مفيد آهي ڪم جا مقصد. |
| توانائي جو سرچشمو 17> | هڪ اليڪٽرولائيٽڪ سيل کي ڪم ڪرڻ لاءِ توانائي جي هڪ خارجي ذريعن جي ضرورت هوندي آهي. هڪ بيٽري ٻنهي اليڪٽروڊس سان ڳنڍيل آهي جيڪي اليڪٽرولائيٽڪ سيل جي ڪم کي شروع ڪن ٿيون. | گليوانڪ يا وولٽڪ سيل کي توانائي جي ڪنهن به ٻاهرين ذريعن جي ضرورت ناهي ڇو ته اها پنهنجي توانائي پيدا ڪري ٿي. |
| چارجز | اليڪٽرولائيٽڪ سيل ۾ منفي طور تي چارج ٿيل انوڊ ۽ مثبت طور تي چارج ٿيل ڪيٿوڊس شامل آهن. | گليوانڪ سيل يا وولٽڪ سيل ۾ مثبت طور تي چارج ٿيل انوڊ ۽ منفي طور تي چارج ٿيل ڪيٿوڊس شامل آهن. |
| رد عمل 17> | اليڪٽرولائيٽڪ سيلز غير معمولي رد عمل کي ڪيميائي توانائي پيدا ڪرڻ لاءِ استعمال ڪن ٿا. اهو برقي توانائي کي ڪيميائي توانائي ۾ تبديل ڪري ٿو. | گليوانڪ يا وولٽائيڪ سيلز غير خود بخود استعمال ڪن ٿابرقي توانائي پيدا ڪرڻ لاء ردعمل. اهو ڪم لاءِ گهربل توانائيءَ کي ڪيميائي توانائيءَ ۾ تبديل ڪري ٿو. |
فرقن جي وچ ۾ گليوانڪ ۽ اليڪٽرولائيٽڪ سيلز
ڏسو_ پڻ: Chidori VS Raikiri: انھن جي وچ ۾ فرق - سڀ فرقاليڪٽرولائيٽڪ سيل جا عملي استعمال
اليڪٽرولائيٽڪ سيل اڄ جي سماج ۾ پاڻ لاء هڪ اهم ڪردار ڪيو آهي ۽ وڏي تعداد ۾ استعمال ڪيو ويندو آهي. اليڪٽرولائيٽڪ سيلز جي عملييت ۽ اهميت هيٺ ڏجي ٿي:
- اهو پگھليل سوڊيم ڪلورائڊ مان سوڊيم ڌاتو تيار ڪرڻ لاءِ استعمال ڪيو ويندو آهي ڊائونس سيل استعمال ڪندي.
- <2 اهو ڪلورين گيس حاصل ڪرڻ لاءِ استعمال ڪيو ويندو آهي س ۽ ڪاسٽڪ سوڊا (NaOH) تيار ڪرڻ لاءِ آبي سوڊيم ڪلورائڊ نيلسن سيل پاران.
- اهو ٽامي جي اليڪٽررو ريفائننگ ۾ استعمال ٿيندو آهي.
- Electrolytic Cells electroplating metals لاءِ استعمال ٿيندا آهن.
- اليڪٽرولائيٽڪ سيل پاڻي مان آڪسيجن گيس ۽ هائيڊروجن گيس پيدا ڪرڻ لاءِ استعمال ڪيو ويندو آهي ان کي اليڪٽرولائيسس ذريعي پهچائڻ. Cells
Galvanic or voltaic Cells اڄ جي دنيا لاءِ هڪ اهم ايجاد آهن ۽ انسان ذات پاران تمام گهڻو استعمال ڪيو وڃي ٿو. بجلي جديد زندگي جي هڪ بنيادي ضرورت آهي ۽ ان جي پيداوار تمام ڏکيو عمل آهي، ان جي باوجود اسان وٽ بجلي پيدا ڪرڻ جا ڪيترائي طريقا آهن.
گليوانڪ يا وولٽڪ سيلز بجلي پيدا ڪرڻ جي ابتدائي طريقن مان هڪ آهن. اهو اڃا تائينبجلي پيدا ڪرڻ جي جديد ۽ جديد طريقن جي وچ ۾ وڏي اهميت رکي ٿو.
- گليوانڪ سيلز جو عمل ڪيترن ئي قسمن جو آهي ۽ ڪيترن ئي طريقن سان انساني زندگي کي متاثر ڪري ٿو. خشڪ سيل يا بيٽريون، جيڪي اسان عام طور تي اسان جي روزاني زندگيءَ ۾ استعمال ڪندا آهيون، اسان جي ٽارچ لائٽ، ٽي وي ڪنٽرول، گيمنگ ڪنٽرولرز ۽ ٻيون ڪيتريون ئي شيون.
- ليڊ اسٽوريج بيٽري پڻ هڪ آهي. روزاني مثال هڪ galvanic سيل جو. ليڊ اسٽوريج بيٽري جو ڪم بجلي پيدا ڪرڻ آهي جڏهن مکيه پاور سپلائي بند آهي. اهو عام طور تي گهرن ۽ ڪم جي جڳهن ۾ بيڪ اپ طور استعمال ڪيو ويندو آهي.
- فيول سيلز وڏي پيماني تي صنعتن ۾ استعمال ڪيا ويندا آهن جيئن انهن جو بيڪ اپ وڏو هجڻ ضروري آهي. اهي استعمال ٿيندا آهن جڏهن بجلي ختم ٿي ويندي آهي ۽ مشينري کي ڪم ڪرڻو پوندو آهي.
Galvanic Cell vs. Electrolytic Cell
Conclusion
- مجموعي طور تي ان کان پوءِ، ٻئي اليڪٽرولائيٽڪ ۽ گليوانڪ يا وولٽڪ سيلز هن جديد دنيا ۾ پروسيسنگ جي پنهنجي منفرد انداز ۾ پنهنجي اهميت رکن ٿا. اهي ٻئي سيل اڃا تائين استعمال ۾ آهن ۽ اڃا تائين پنهنجي مقصد کي پورو ڪري رهيا آهن.
- مجموعي طور تي، اهو طريقو جيڪو ٻنهي اليڪٽرولائيٽڪ ۽ گليوانڪ سيلز جي پيداوار کان گذري ٿو سادو آهي ۽ عام ماڻهو تائين آساني سان پهچندو آهي.
- اليڪٽرولائيٽ سيل ڪم نٿو ڪري سگهي جڏهن اهو ڪنهن به ٻاهرين پاور سپلائي سان ڳنڍيل ناهي. ان جي ابتڙ، galvanic ڪليڪشن کي ڪنهن به خارجي بجلي جي فراهمي سان ڳنڍڻ جي ضرورت ناهي جيئن اها پيدا ٿئي ٿي.پنهنجي طاقت.
- ٻنهي سيلن جو استعمال هاڻي سڄي دنيا ۾ مشهور ۽ واقف آهي، ۽ هي شاندار ايجاد هاڻي نوجوانن جي نصاب جو حصو آهي ۽ اڄڪلهه هر ٻار کي سيکاريو وڃي ٿو.

